Business
製薬業IT
コンサルティング
HOME > 製薬業ITコンサルティング
ビュルガーコンサルティングは、IT化支援を通して、
製薬企業様のビジネス革新に貢献します。
私たちは、長年にわたり、数々の製薬企業様の様々なIT化をご支援してきており、製薬企業様を取り巻く環境の変化や抱える課題を共有しているため、最適なIT化の実現をご支援できます。私たちは、IT化支援を通して、製薬企業様のビジネス革新に貢献し、これにより、優れた薬を待つ患者様のお役に立ちたいと、心から願っています。私たちがご支援してきた、製薬企業様のIT化の主な対象領域をご紹介させていただきます。
文書管理システム 導入支援
eCTD(新薬の電子申請)に向けた文書管理に取り組んできた、豊富な経験とノウハウを持つコンサルタントが、eCTD対応プロセス・システム構築支援を行います。またeCTDだけではなく、SOPや計画書/報告書、製品標準書、添付文書 等、各種の文書の電子化支援を行います。
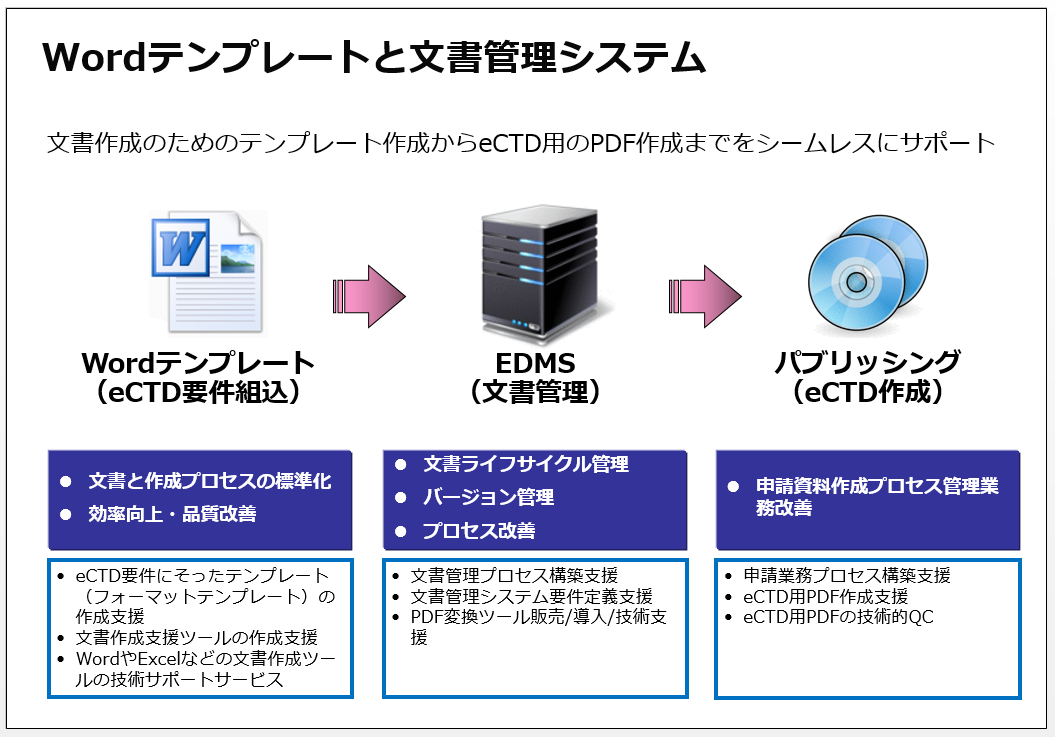
Wordテンプレート 導入支援
現場の執筆者が抱える申請文書作成時の課題の詳細まで熟知し、豊富な専門スキルを持つコンサルタントが、数々の事例を踏まえた最適な解決策であるWordテンプレートの提供を中心とした申請文書作成の品質と効率の向上支援を行います。
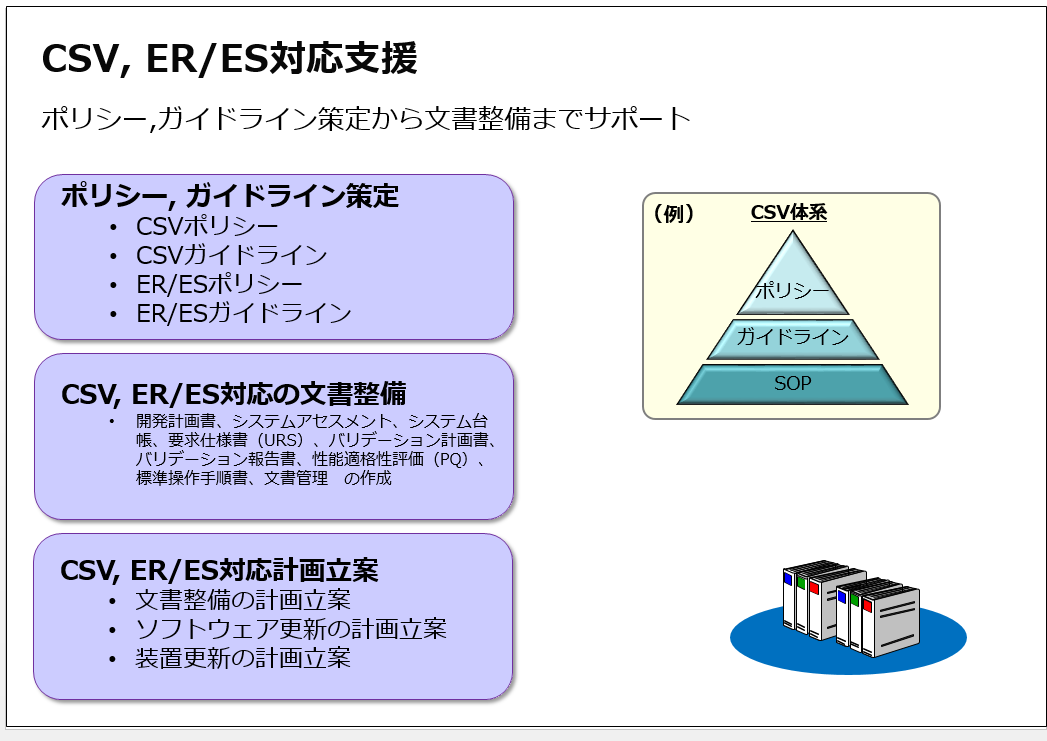
CSV、ER/ES 対応支援
これまで数々の製薬企業様のCSVのポリシーやガイドライン、またER/ES対応のポリシーやガイドラインの検討に取り組んできたコンサルタントが、これらのポリシーやガイドラインの策定の支援を行います。また文書管理、eCTD、 CSV(Part11対応)、ER/ESのトレーニングも行います。
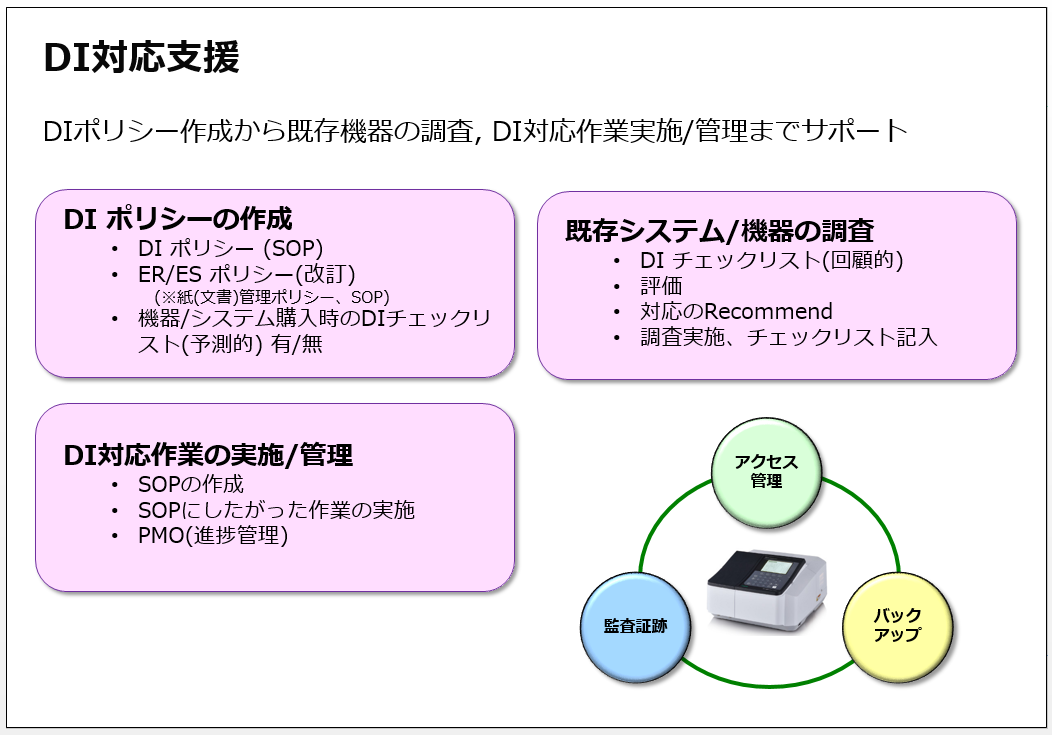
DI(データインテグリティー) 対応支援
現在、取り組みが急務となっている、DI(データインテグリティー)への対応を、これまで製薬企業様でDI対応に取り組んできたコンサルタントがご支援します。DIポリシー/SOP作成、ER/ESポリシー/SOP改定、紙文書管理ポリシー/SOP改定、機器/システム購入時のDI対応チェックリスト作成、既存の機器/システムのDI対応チェック・評価・対応策策定などをご支援します。
グループ監査の実施
製薬企業様では、ITシステムを導入する場合に、そのベンダーの監査が必要になります。ビュルガーはその監査のご支援を行います。同じITシステムを複数の製薬企業様でご使用の場合、複数社の共同でベンダー監査を行う、「グループ監査」という形式でも、ビュルガーはご支援することができます。グループ監査に参加する製薬企業様は、コストを抑えることができる上、標準化された監査項目で抜け漏れなく監査を行うことができます。
品質イベント管理システム 導入支援
GMP、 治験薬GMP、 GQPの品質イベント管理に取り組んできたコンサルタントが、イベント管理システム構築に向けた業務要件の整理などのご支援を行います。逸脱管理、変更管理、CAPA、苦情管理、監査等の各種の業務の品質イベント管理システムの導入検討、 構築、 運用の支援を行います。
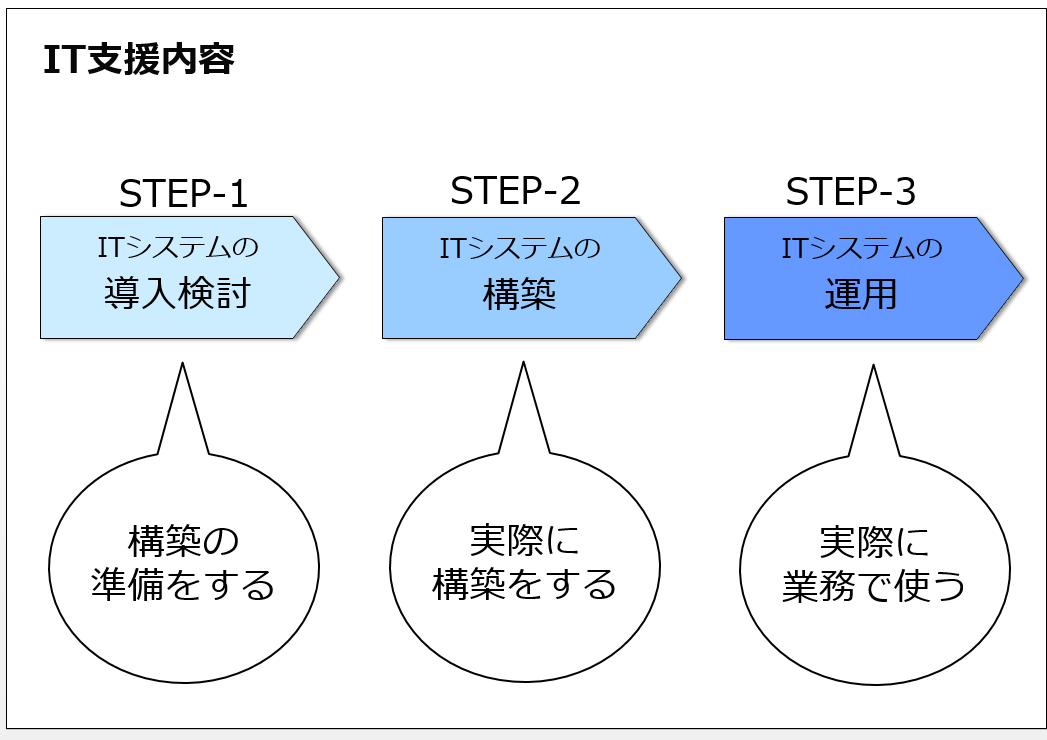
IT支援内容
また、ITシステムの種類を問わず、導入検討支援、構築支援、運用支援を行います。
そのご支援の主な内容は以下の通りです。
ITシステムの導入検討
ITシステムを導入するにあたって、製薬企業様は、対象業務の整理、ベンダー選定(提案依頼書作成、提案比較資料作成、選定結果資料作成)、要件定義などの導入に伴う検討活動が必要になります。こうした活動の支援を行います。
ITシステムの構築
ITシステムを構築するにあたって、製薬企業様は、要件がITシステムの機能や設定に展開されていることを確認し、ユーザー受入れテストを計画し、実施し、報告する必要があります。またマニュアルや教育資料を作成し、ユーザーに教育を実施する必要があります。またCSV活動を実施し、その活動を文書化する必要があります。こうした活動の支援を行います。
ITシステムの運用
ITシステムを運用するにあたって、製薬企業様は、ITシステムを活用した業務運用を検討し、ルール化し、運用体制を組み、運用業務を開始する必要があります。またITシステムの変更管理や逸脱管理などを実施する必要があります。こうした活動の支援を行います。
事例紹介
ビュルガーコンサルティングがご支援してきた、製薬企業様IT化支援の事例の一部をご紹介させていただきます。
文書管理システム 導入支援
| 事例 | eCTD対応の申請文書管理システムの導入支援 |
|---|---|
| お客様 | 大手製薬企業様:R&D、薬事、QA、ITの各部門 |
| お客様の課題 | 新eCTDシステム構築のための申請文書作成業務プロセスの再構築とITシステム構築 |
| コンサル内容 | 豊富な他社事例・業界動向を示しながら、判断の難しい点を効果的にガイドしてプロジェクトを推進 |
| 成果 | 品質の高い最適なプロセスとシステム要件の定義が達成でき、予定通りに新システムを導入 |
Wordテンプレート 導入支援
| 事例 | eCTD対応のWordテンプレートの導入支援 |
|---|---|
| お客様 | 大手製薬企業様:R&D、薬事、QA、ITの各部門 |
| お客様の課題 | 申請文書作成の品質と効率の両方の向上を実現すること |
| コンサル内容 | 豊富な経験事例と専門スキルにより、お客様を的確にサポートしてWordテンプレートの作成と訓練を実施 |
| 成果 | Wordテンプレートの活用により、Word機能に迷うことなく、標準化された高品質の文書作成を実現 |
CSV、ER/ES 対応支援
| 事例 | ER/ESポリシー、ガイドライン策定支援 |
|---|---|
| お客様 | 大手製薬企業様:CSV担当チーム |
| お客様の課題 | ER/ESのポリシー、ガイドラインが社内に存在しないので、ER/ESに対応したITや業務であると説明するのが困難 |
| コンサル内容 | 豊富な他社事例・業界動向を示しながら、判断の難しい点を効果的にガイドしてプロジェクトを推進 |
| 成果 | 規制要件と社内状況の両方を踏まえた、最適なER/ESポリシーとガイドラインを策定し、社内へのトレーニングも実施 |
DI(データインテグリティー) 対応支援
| 事例 | DI対応支援 |
|---|---|
| お客様 | 大手製薬企業様:品質管理部門 |
| お客様の課題 | DI対応チェック項目が整備されていないため、社内の機器のDI対応チェック・評価・対応の検討が困難 |
| コンサル内容 | 他社事例・業界動向を示しながら、判断の難しい点を効果的にガイドしてプロジェクトを推進 |
| 成果 | 規制要件と社内状況の両方を踏まえ、最適なDI対応チェック項目を整備し、機器調査支援も実施 |
グループ監査の実施
| 事例 | グループ監査 |
|---|---|
| お客様 | JSQA(日本QA研究会)の複数の製薬企業様 |
| お客様の課題 | 富士通社のDDworks21(クラウドサービス)のベンダー監査を実施したい。 コストや工数を抑えて実施したい。 |
| コンサル内容 | ヒアリング項目を整備してベンダーに提示し、回答を受けた上で、実地調査を実施。これらの活動をまとめて監査報告書を作成 |
| 成果 | 規制要件と各社利用状況の両方を踏まえ、最適なベンダーチェック項目を作成して回答を得た。実地調査も実施した。 |
品質イベント管理システム導入支援
| 事例 | GMPのイベント管理システムの導入検討・構築支援 |
|---|---|
| お客様 | 大手製薬企業様:GMP、QA、ITの各部門 |
| お客様の課題 | GMPのイベント(逸脱、変更、CAPA)管理の業務プロセス再構築とITシステム構築 |
| コンサル内容 | 他社事例を示しつつ、判断の難しい点を効果的にガイドしてプロジェクトを推進 |
| 成果 | 品質の高い最適なプロセスとシステム要件の定義が達成でき、予定通りに新システムを導入 |
講師実績
ビュルガーコンサルティングのコンサルタントが実施したセミナー講師の実績の一部をご紹介させていただきます。
| セミナー名 | 講演日時 | 講演タイトル | 講演者 |
|---|---|---|---|
| 情報機構セミナー | 2009年6月9日 | 『eCTD対応のリーフファイル作成講座』 | 神津 陽一 |
| 技術情報協会セミナー | 2009年11月26日 | 『eCTD申請に対応したドキュメント管理』 | 吉村 健 |
| eCTD研究会 第2回教育セミナー | 2011年10月11日 | 『文書管理の考え方と文書管理システムについて』 | 吉村 健 |
| 第2回eCTDシンポジウム | 2013年7月9日 | 『文書管理システムの重要性と動向について』 | 吉村 健 |
| eCTD研究会 担当者養成コース | 2013年度~2016年度(2017年度も同様の講義を実施予定) | 『eCTDにおける文書管理の考え方』 | 吉村 健 |
| 医薬品・医療機器業界向けセミナー | 2015年4月15日 | 事例で見るQMS(品質管理システム)電子化のポイント 『品質イベント管理の電子化にあたってユーザー側が行うこと』 | 山岸 幸満 |
| PharmaDocユーザー会 | 2015年5月29日 | 『クラウド時代のバリデーション』 | 吉村 健 |
| Veeva SUMMIT | 2016年5月19日 | 『eCTDにおける文書管理の考え方』 | 吉村 健 |
| eCTD研究会第11 回セレクト講座 | 2016年11月10日 | 『Word 利用に関するよくある質問や活用法』 | 神津 陽一 |
紹介記事
ビュルガーコンサルティングの紹介記事の一部をご紹介させていただきます。
| 書籍名 | 記事内容 |
|---|---|
| 『eCTD提出状況、eCTDツール、委託先』(日本製薬工業協会 eCTD研究会, 2008年5月15日) | 試験報告書(総括報告書)のDraft執筆後の電子的点検の委託先として、弊社を紹介 (P.14) |
| 『月間 PHARM STAGE』(技術情報協会, 2008年7月号) | 「eCTD講座」において、製薬業界在籍の著名な執筆者が、eCTD申請文書のテンプレートのベンダーとして弊社を紹介。「ビュルガーコンサルティングでは、数社の製薬会社のテンプレート作成や執筆者教育の経験があり、テーラーメイドでのテンプレート作成を請け負っている。」(P.120)また「Word文書がeCTD規制要件に適合しているかの電子的QCを行うツールの開発ベンダー」としても紹介。P.122) |
執筆書籍紹介
ビュルガーコンサルティングのコンサルタントが執筆した書籍の一部をご紹介させていただきます。
| 書籍名 | タイトル | 執筆者 |
|---|---|---|
| 『~欧・米・中、日本を中心とした~ 世界への薬事申請書の書き方 | 第5部 第2章 6節 2項 eCTD作成におけるER/ES規制 |
山岸 幸満 |
| 成功へのバイブル ≪ 医薬品・医療機器・体外診断薬 ≫』 (株式会社 技術情報協会、2012/12/28発刊) |
対応のポイント | |
| 『~欧・米・中、日本を中心とした~ 世界への薬事申請書の書き方 成功へのバイブル ≪ 医薬品・医療機器・体外診断薬 ≫』 (株式会社 技術情報協会、2012/12/28発刊) |
第5部 第2章 6節 4項 ドキュメント 管理システムの構築と管理手法 |
吉村 健 |
| 『医薬品・医療機器の開発・製造におけるコンピュータ化システム適正管理対応実務とドキュメント作成事例集』 (株式会社 技術情報協会、2013/3/31発刊) |
第2部 第3章 第5節 臨床試験におけるコンピュータ化システムのリスク評価の考え方 | 吉村 健 山岸 幸満 |
| 『臨床開発における電子化とCSV対応の進め方』 (株式会社 情報機構、2013/6/30発刊) |
11.既存システムのバリデートのアプローチ | 吉村 健 山岸 幸満 |
